臭氧的性质
一、 臭氧的物理性质
臭氧是一种具有刺激性特殊气味的不稳定气体,分子结构如图所示。它可在地球同温层内光化学合成,但是在地平面上仅以极低浓度存在。
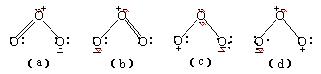
共振杂化分子的四种典型形
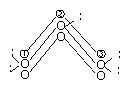
一种简化的分子轨道图
1.1 一般物理性质
在常温下,臭氧为蓝色气体,不过在常温下,蓝色并不明显,除非是相当厚的气体。臭氧的主要物理性质列于表
1-1, 液体密度和蒸汽压列于表 1-2 。
1-1 纯臭氧的物理性质
|
熔点( 760mmHg)/℃ |
-192.5±0.4 |
气体密度( 0℃)/(g/L) |
2.144 |
|
沸点( 760mmHg)/℃ |
-111.9±0.3 |
蒸发热( -112℃)/(J/L) |
316.8 |
|
临界温度 /℃ |
-12.1 |
临界密度 /(g/ml) |
0.437 |
|
临界压力 /atm |
54.6 |
固态臭氧密度( 77.4K)
(g/cm 3 ) |
1.728 |
|
临界体积( cm 3 /mol) |
111 |
液态热容( 90~105K) (cal/k) |
0.425+0.0014×(T-9) |
|
液态臭氧的粘滞度 77.6K(Pa・s)
90.2K(Pa・s) |
0.00417 0.00156 |
汽化热 -111.9℃
-183℃ |
14277
15282 |
|
表面张力( cyn/cm)①
77.2K
90.2K |
43.8 38.4
|
生成热 气体( 298.15k)
液体( 90.15k)
理想气体( 0k) |
142.98
125.60
145.45
|
|
等张比容( 90.2K) |
75.7 |
生成自由能(气体, 298.15k) |
162.82 |
|
介电常数(液态 90.2k) |
4.79 |
偶极距 /Debye(德拜) |
0.55 |
|
磁化率( cm-g-s单位)气体/液体 |
0.002×10 -6 0.150 |
|
|
①1dyn=10 -3 N/m;1atm=101.325Pa;1cal=4.18J 。
表 1-2 臭氧的液体密度和蒸气压
| 温度
/℃ |
液体密度/(g/cm 3 ) |
液体蒸气/mmHg |
温度
/℃ |
液体密度/(g/cm 3 ) |
液体蒸气/mmHg |
|
-183 |
1.574 |
0.11 |
-140 |
1.442 |
74.2 |
|
-180 |
1.566 |
0.21 |
-130 |
1.410 |
190 |
|
-170 |
1.535 |
1.41 |
-120 |
1.318 |
427 |
|
-160 |
1.504 |
6.75 |
-110 |
1.347 |
865 |
|
-150 |
1.473 |
24.3 |
-100 |
1.316 |
1605 |
1.2 ,
臭氧略溶于水,标准压力和温度下( STP ),其溶解度比氧大 13 倍(见表 1-3 ),比空气大 25
倍。
表 1-3 臭氧在水中的溶解度(气体分压为 10 5 Pa ) /(ml/L)
|
气体 |
密度( g/L) |
温度
/℃ |
| 0 |
10 |
20 |
30 |
| O 2 |
1.492 |
49.3 |
38.4 |
31.4 |
26.7 |
| O 3 |
2.143 |
641 |
520 |
368 |
233 |
| 空气 |
1.2928 |
28.8 |
23.6 |
18.7 |
16.1 |
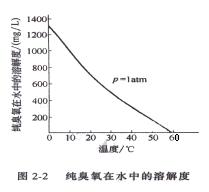
将臭氧通入蒸馏水中,可以测出不同温度、不同压力下臭氧在水中的溶解度。图 2-2 是在压力为 1atm
时,纯臭氧在水中的溶解度和温度的关系曲线。从图2-2 知,当温度为 0℃ 时,纯臭氧在水中的溶解度可达
2.858×10 -2 mol/L(1372mg/L).
臭氧和其他气体一样,在水中的溶解度符合亨利定律,即在一定温度下,任何气体溶解于已知液体中的质量,将与该气体作用在液体上的分压成正比,而亨利常数的大小只是温度的函数,与浓度无关。
C=K H P (1-1)
式中 C -臭氧在水中的溶解度, mg/L ;
P -臭氧化空气中臭氧的分压, kPa ;
K H -亨利常数, mg/ ( L・kPa )。
从式( 1-1 )知,由于实际生产中采用的多是臭氧化空气,其臭氧的分压很小,故臭氧的溶解度远远小于表
1-3 中的数据。例如,用空气为原料的臭氧发生器生产的臭氧化空气,臭氧只占 0.6 %~ 1.2
%(体积)。根据气态方程及道尔顿分压定律知,臭氧的分压也只有臭氧化空气压力的 0.6 %~ 1.2
%。因此,当水温为 25℃ 时,将这种臭氧化空气加入水中,臭氧的溶解度只有( 0.625 ~ 1.458 )
×10 -4 mol/L(3 ~ 7mg/L) 。
表 1-4 低浓度臭氧在水中的溶解度 /(mg/L)
|
气体质量百分比含量/% |
温度 /℃ |
| 0 |
5 |
10 |
15 |
20 |
25 |
30 |
| 1 |
8.31 |
7.39 |
6.5 |
5.6 |
4.29 |
3.53 |
2.7 |
| 1.5 |
12.47 |
11.09 |
9.75 |
8.4 |
6.43 |
5.09 |
4.04 |
| 2 |
16.64 |
17.79 |
13 |
11.19 |
8.75 |
7.05 |
5.39 |
| 3 |
24.92 |
22.18 |
19.5 |
16.79 |
12.86 |
10.58 |
8.09 |
在一般水处理中,臭氧浓度较低,所以在水中的溶解度并不大。在较低浓度下,臭氧在水中的溶解度基本满足亨利定律。低浓度臭氧在水中的溶解度见表
1-4 。
二、臭氧的化学性质
1. 臭氧的化学性质极不稳定,在空气和水中都会慢慢分解成氧气,其反应式为:
2O3 →3O2 + 285kJ ( 1-2 )
由于分解时放出大量热量,故当其含量在 25 %以上时,很容易爆炸。但一般臭氧化空气中臭氧的含量很难超过 10
%,在臭氧用于饮用水处理的较长历史过程中,还没有一例氧爆炸的事例。
含量为 1 %以下的臭氧,在常温常压的空气中分解半衰期为 16h 左右。随着温度的升高,分解速度加快,温度超过
100℃ 时,分解非常剧烈,达到 270℃
高温时,可立即转化为氧气。臭氧在水中的分解速度比空气中快的多。在含有杂质的水溶液中臭氧迅速回复到形成它的氧气。如水中臭氧浓度为
6.25×10 -5 mol/L(3mg/l) 时,其半衰期为 5 ~ 30min
,但在纯水中分解速度较慢,如在蒸馏水或自来水中的半衰期大约是 20min ( 20℃
),然而在二次蒸馏水中,经过 85min 后臭氧分解只有 10 %,若水温接近 0℃ 时,臭氧会变得更加稳定。
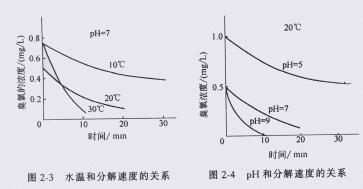
臭氧在水中的分解速度随水温和 PH 值的提高而加快,图 2-3 为 PH=7
时,水温和分解速度的关系,图 2-4 为 20℃ , PH 和分解速度的关系。
为提高臭氧利用率,水处理过程中要求臭氧分解得慢一些,而为了减轻臭氧对环境的污染,则要求处理后尾气中的臭氧分解快一些。
2. 臭氧的氧化能力
臭氧得氧化能力极强,其氧化还原电位仅次于 F 2 ,在其应用中主要用这一特性。从表 1-5 中看出。
从表 1-5
可知,臭氧的标准电极电位除比氟低之外,比氧、氯、二氧化氯及高锰酸钾等氧化剂都高。说明臭氧是常用氧化剂中氧化能力最强的。同时,臭氧反应后的生成物是氧气,所以臭氧是高效的无二次污染的氧化剂。
表 1-5 氧化还原电位比较
| 名称 |
分子式 |
标准电极电位 /mv |
名称 |
分子式 |
标准电极电位 /mv |
| 氟 |
F2 |
2.87 |
二氧化氯 |
ClO 2 |
1.50 |
| 臭氧 |
O3 |
2.07 |
氯 |
Cl 2 |
1.36 |
| 过氧化氢 |
H2O2 |
1.78 |
氧 |
O 2 |
1.23 |
| 高锰酸钾 |
MnO4 - |
1.67 |
|
|
|
3. 臭氧的氧化反应
a 、与无机物的氧化反应
⑴ 臭氧与亚铁的反应
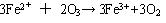
⑵ 臭氧与 Mn2+ 的反应
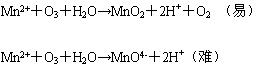
⑶ 臭氧与硫化物的反应
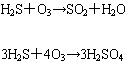
⑷ 臭氧与硫氰化物的反应

⑸ 臭氧与氰化物的反应
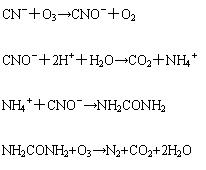
总反应为:

⑹ 臭氧与氯的反应
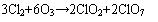
b 、臭氧与有机物的反应
臭氧在水溶液中与有机物的反应极其复杂,下面仅以大家公认的几种反应式列出以供参考。
⑴ 臭氧与烯烃类化合物的反应 臭氧容易与具有双链的烯烃化合物发生反应,反应历程描述如下:
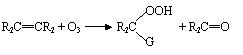
式中 G 代表 OH 、 OCH3 、 OCCH3
等基。反应的最终产物可能是单体的、聚合的、或交错的臭氧化物的混合体。臭氧化物分解成醛和酸。
⑵ 臭氧和芳香族化合物的反应
臭氧和芳香族化合物的反应较慢,在系列苯<萘<菲<嵌二萘<蒽中,其反应速度常数逐渐增大。其
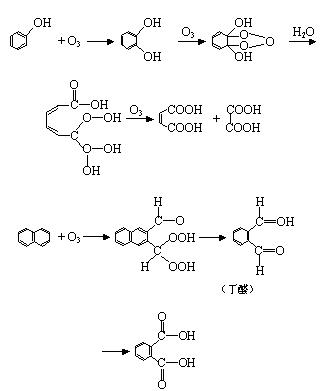
⑶ 对核蛋白(氨基酸)系的反应

⑷ 对有机氨的氧化
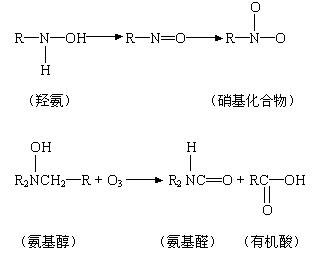
臭氧在下列混合物的氧化顺序为
链烯烃>胺>酚>多环芳香烃>醇>醛>链烷烃
c 、臭氧的毒性和腐蚀性
臭氧属于有害气体,浓度为 6.25×10 -6 mol/L(0.3mg/m3 )
时,对眼、鼻、喉有刺激的感觉;浓度 (6.25-62.5)×10 -5 mol/L(3 ~ 30mg/m3 )
时,出现头疼及呼吸器官局部麻痹等症 ; 臭氧浓度为 3.125×10 -4 ~ 1.25×10 -3
mol/L(15 ~ 60mg/m 3 ) 时 , 则对人体有危害。其毒性还和接触时间有关,例如长期接触
1.748×10 -7 mol/L(4ppm) 以下的臭氧会引起永久性心脏障碍,但接触 20ppm
以下的臭氧不超过 2h ,对人体无永久性危害。因此,臭氧浓度的允许值定为 4.46×10 -9
mol/L(0.1ppm)8h. 由于臭氧的臭味很浓,浓度为 4.46×10 -9 mol/L(0.1ppm)
时,人们就感觉到,因此,世界上使用臭氧已有一百多年的历史,至今也没有发现一例因臭氧中毒而导致死亡的报道。
臭氧具有很强的氧化性,除了金和铂外,臭氧化空气几乎对所有的金属都有腐蚀作用。铝、锌、铅与臭氧接触会被强烈氧化,但含铬铁合金基本上不受臭氧腐蚀。基于这一点,生产上常使用含
25 % Cr 的铬铁合金(不锈钢)来制造臭氧发生设备和加注设备中与臭氧直接接触的部件。
臭氧对非金属材料也有了强烈的腐蚀作用,即使在别处使用得相当稳定得聚氯乙烯塑料滤板等,在臭氧加注设备中使用不久便见疏松、开裂和穿孔。在臭氧发生设备和计量设备中,不能用普通橡胶作密封材料,必须采用耐腐蚀能力强的硅橡胶或耐酸橡胶等。